
手機掃碼訪問本站

微信咨詢
特立帕肽是一種合成的34肽,為人甲狀旁腺素PTH的1-34氨基酸片段,氨基酸順序 如下:H-Ser1-Val2-Ser3-Glu4-Ile5-Gln6-Leu7-Met8-His9- Asn10-Leu11-Gly12-Lys13-His14-Leu15-Asn16-Ser17-Met18-Glu19-Arg20-Val21-Glu22-Trp23-Leu24-Arg25-Lys26-Lys27-Leu28-Gln29-Asp30-Val31-His32-Asn33-Phe34-OH。該片段是含有84個氨基酸的內源性甲狀旁腺素PTH具有生物活性的N-末端區域。 本品的免疫學和生物學特性與內源性甲狀旁腺素PTH以及牛甲狀旁腺素PTH(bPTH)完全相同。特立帕肽是第一種獲得美國食品及藥物管理局FDA批準的骨形成劑類新藥,這種甲狀旁腺激素的衍生物可以通過增加成骨細胞的活性及數量而促進骨生長,而目前的常規骨質疏松藥物一般只是作用于破骨細胞而減緩或阻斷骨質流失,醋酸特立帕肽是由禮來藥廠生產的,涉及到1637例絕經后骨質疏松癥患者的臨床研究結果顯示,與那些只服用了鈣和維 生素D補加劑的患者相比,96%的患者在接受該藥治療后,其脊柱和臀部的骨(礦物質)密度 BMD均表現出顯著增加,此外還發現,該藥能夠分別減少發生脊柱骨折和其他類型骨折危險 的65%和53%。

美國FDA批準用于絕經后女性骨質疏松癥以及高度骨折風險的男性骨質疏松癥(包括性腺功能減退引起的繼發性骨質疏松癥)的治療。對22例絕經后骨質疏松癥婦女分別應用特立帕肽20 μg· d-1與每周利塞膦酸鈉35 mg,在開始治療前、治療后第3個月、第6個月觀察骨轉換指標改變,1年后停用藥物。研究發現,反映骨形成相關指標如血清堿性磷酸酶(ALP)、Ⅰ型原膠原N端前肽(PINP)在特立帕肽組明顯增加(P<0.001),而在利塞膦酸鈉組明顯下降(P<0.001);反映骨吸收指標血清Ⅰ 型膠原C端肽(CTX)在特立帕肽組也增加,而在利塞膦酸鈉組下降,提示特立帕肽獨特促進骨形成與骨吸收的雙重作用。本品是目前已上市藥物中惟一促進骨形成的藥物,我國正在進行該藥的Ⅳ期臨床試驗。
目前原發性骨質疏松癥常規治療藥物如雙膦酸鹽、降鈣素、雌激素類,作用機制均是通過抑制破骨細胞活性達到治療骨質疏松癥效果,而特立帕肽是目前惟一認為具有促進骨合成代謝的藥物。單獨或聯合應用特立帕肽,可以增加骨密度、改善骨微結構、降低骨折風險。多數臨床研究均證明,特立帕肽增加骨密度作用呈劑量依賴性增加,雖然40 μg·d-1組增加骨密度效果優于20 μg·d-1組,但是并沒有進一步降低骨折風險,且不良反應風險可能更大。
1)特立帕肽與雙膦酸鹽
多項臨床試驗證明特立帕肽增加骨密度、減少骨折風險作用強于阿侖膦酸鈉。目前臨床不推薦本品與雙膦酸鹽聯用。在83 例腰椎骨密度降低男性患者中發現單獨應用特立帕肽治療后,其骨密度增加效果不但優于單用阿侖膦酸鈉治療,也優于兩者聯合治療。研究中同時發現使用阿侖膦酸鈉后骨形成標志物骨鈣素(BGP),PINP和骨吸收標志物CTX均有所下降,隨著特立帕肽的加入這些標志物濃度才有所上升,推測特立帕肽促進骨形成的作用會受到阿侖膦酸鈉的不利影響。但目前大多數研究支持雙膦酸鹽類作為特立帕肽結束治療后下一步治療的選擇藥物。
2)特立帕肽與選擇性雌激素受體調節劑
將137 例絕經后骨質疏松癥婦女分為2組,一組接受特立帕肽20 μg· d-1及雷洛昔芬60mg· d-1聯合治療,另一組單獨應用特立帕肽20 μg·d-1,觀察6個月后發現兩組PINP水平均明顯升高,兩組相比無統計學差異;而CTX的濃度在聯合治療組低于單用特立帕肽組(P=0.015),提示本品聯合應用雷洛昔芬可以在促進骨形成的同時抑制骨吸收;兩組骨密度較治療前基線水平均明顯上升,但聯合治療組髖部骨密度增加較單用特立帕肽組更明顯(P=0.04);聯合治療組不良反應發生率與單用特立帕肽組相似,推測聯合應用雷洛昔芬可以加強特立帕肽促成骨的作用。因此單用雌激素受體調節劑治療效果不佳的患者可以考慮聯合本品治療。
3)特立帕肽與降鈣素
對亞洲地區63例絕經后骨質疏松的婦女隨機分成2組,分別接受特立帕肽20 μg· d-1及降鈣素100 IU· d-1治療,6個月后發現特立帕肽治療組脊柱骨密度較降鈣素組明顯增加,且骨轉換指標改變更加明顯(骨特異性ALP142% vs37%;骨鈣素154% vs23%,P<0.001),顯示特立帕肽組促進骨形成作用要優于降鈣素。目前還沒有本品與降鈣素聯用的相關文獻報道。且無研究支持降鈣素作為特立帕肽治療結束后的后續治療藥物。
4)與維生素D和鈣劑聯用
對絕經后骨質疏松癥婦女研究發現,在鈣劑和維生素D使用基礎上,同時接受特立帕肽20 μg· d-1,統計結果顯示鈣劑與維生素D聯用特立帕肽可以增加腰椎骨密度并降低非椎體骨折風險,因此考慮本品與上述兩種藥物聯用具有協同作用。
通過骨密度檢查篩選出437例男性原發性骨質疏松癥或性腺功能減退引起的繼發性骨質疏松癥患者,隨機分為3組(安慰劑組、特立帕肽20和40 μg· d-1組)。所有患者均接受鈣劑與維生素D的基礎治療。11個月觀察期結束后,特立帕肽20與40 μg· d-1組患者腰椎骨密度分別增加了5.9%與9.0%(與安慰劑組相比P<0.001),股骨頸骨密度增加了1.5%(P=0.029)和2.9%(P<0.001),同時觀察到40 μg· d-1組不良反應高于20μg· d-1組。后續研究中將其中350例男性骨質疏松癥患者繼續觀察30 ~ 42個月,發現特立帕肽組椎體骨折發生率較安慰劑組降低51%。目前臨床常用治療糖皮質激素誘導的繼發性骨質疏松癥藥物包括雙磷酸鹽和降鈣素類。觀察428例糖皮質激素誘導的骨質疏松癥患者(每日服用潑尼松劑量≥5 mg,時間≥ 3個月),214例給予特立帕肽20 μg· d-1,214例給予阿侖膦酸鈉10 mg· d-1,治療6個月后兩組腰椎骨密度增加幅度即出現統計學顯著差異,且特立帕肽組腰椎骨折發生率明顯低于阿侖膦酸鈉組,但至少有1次血清鈣測量值升高的患者,在特立帕肽組顯著多。因此本品是治療糖皮質激素繼發骨質疏松癥極有前景的藥物。
特立帕肽皮下注射后吸收及消除速度都很快,皮下注射本品20 μg,達峰時間(tmax)為30 min,半衰期(t1/2 )為60 min,靜脈注射血清半衰期為5 min,絕對生物利用度95%。90%藥物經腎臟清除。目前進行的臨床研究多以皮下注射為給藥方式。對10 名健康受試者比較肺部給藥1 600 IU與皮下注射400 IU在達峰時間與峰濃度的差異,結果表明,肺部給藥達峰時間為(10 ±5)min,快于皮下注射給藥達峰時間(28 ±8)min;肺部給藥峰濃度為(309 ±215)pmol· L-1,高于皮下注射給藥峰濃度(102 ±45)pmol· L-1,生物利用度為48%,因此認為肺部給藥是有效的,也是有可能代替皮下給藥的途徑之一。Nastech制藥公司研發的人甲狀旁腺激素鼻噴劑PTH(1-34)目前已進入Ⅱ期臨床試驗,其生物利用度與皮下注射特立帕肽相似。
特立帕肽注射后常見不良反應包括頭暈、背痛、惡心和下肢痙攣等,多為一過性;少見的不良反應包括心律失常、耳聾等。目前認為不良反應發生與患者年齡和給藥劑量之間無明顯關系。在大鼠研究中發現特立帕肽使骨腫瘤如骨肉瘤發生率增加,并且腫瘤發生與給藥劑量與治療持續時間相關。但美國FDA認為大鼠實驗模型并不能真實代表人體研究的結果,該藥于2002年12月獲FDA批準上市。在上市后進行的為期3年的前瞻性的臨床研究,并未發現使用特立帕肽使患者骨腫瘤發病率有所增加。但是目前仍建議在應用特立帕肽時,具有骨肉瘤潛在危險性的對象如Paget骨病、骨骼放療史的患者應避免應用。總結了該藥上市5年來相關安全性的報道以及自身應用的臨床經驗,還發現特立帕肽可引起一過性血鈣升高、高尿鈣和高尿酸血癥,但發生率與安慰劑組比較無顯著性差異。內源性PTH在特立帕肽每天1次20 μg皮下注射給藥后立即出現了持續急劇下降,考慮可能是特立帕肽抑制了甲狀旁腺釋放內源性PTH,并認為其氨基端也可能參與了這個負反饋。當停藥6個月后內源性PTH水平較用藥時上升。因此認為內源性PTH可作為特立帕肽用藥監測的選擇性指標。長期超生理劑量PTH對骨吸收作用大于骨形成,因此尋找治療骨質疏松癥的最佳劑量尤為重要。雖然多數臨床研究均證明本品增加骨密度作用呈劑量依賴性增加,但是考慮安全性與不良反應的因素,目前臨床常用的劑量為20 μg· d-1,并建議使用時間一般不超過2年。
醋酸立特帕肽制備如下:
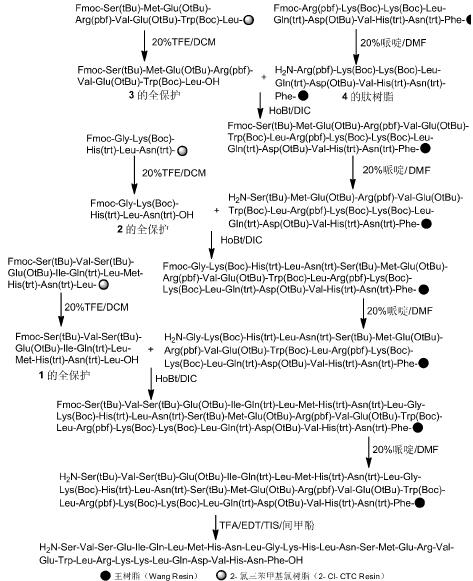
( 1) 4 的肽樹脂的合成
Fmoc-Phe-Wang Resin 的制備: 將Wang Resin15.0 g 加入多肽合成反應柱中,加入DMF 100mL,溶脹30 min; 抽濾,除去濾液。在燒杯中加入Fmoc- Phe-OH 5.8 g( 15 mmol) 、1-羥基苯并三唑( HoBt) 2.4 g( 18 mmol) 和DMF 90 mL,攪拌使其溶解; 冰浴冷卻15 min,加入N,N-二異丙基碳二亞胺( DIC) 2.8 mL( 18 mmol),冰浴活化2 ~ 8 min后加入反應柱中,于30 ℃反應15 min。緩慢滴加4-二甲氨基吡啶( DMAP) 0.18 g ( 1.5 mmol) 的DMF( 10 mL) 溶液,滴畢,反應2 h。除去液體,用DMF( 3 × 30 mL) 洗滌,加入封閉液( 醋酐/吡啶=20 /5,V /V) 100 mL,封閉5 h。除去液體,依次用DMF( 5 × 20 mL) 和MeOH( 3 × 30 mL) 洗滌( 每次10 min),抽干樹脂,真空干燥過夜得Fmoc-Phe-Wang Resin 18.6 g,替代度[11]0.32 mmol·g - 1。肽鏈的延伸: 將Fmoc-Phe-Wang Resin 15.6 g( 5 mmol) 加入反應柱中,根據Fmoc 固相多肽合成原理,以HoBt /DIC 為縮合體系,DMF 為反應溶劑,按2 eq.投料,依次縮合Fmoc-Asn ( trt) -OH、Fmoc-His( trt) -OH、Fmoc- Val-OH、Fmoc-Asp( Ot-Bu ) -OH、Fmoc-Gln ( trt ) -OH、Fmoc-Leu-OH、Fmoc-Lys ( Boc ) -OH、Fmoc-Lys ( Boc ) -OH 和Fmoc-Arg( pbf) -OH,縮合過程中使用Kaiser 法判斷反應終點,最終得4 的肽樹脂28.6 g; MS( ESI) m/z: 1 285.6{ [M + H]+ } 。
2)3 的全保護肽的合成
Fmoc-Leu-CTC Resin 的制備: 將2-Cl-CTC 樹脂20 g( 1.0 mmol·g - 1 ) 加入多肽合成反應柱中,加入DMF 150 mL,溶脹30 min; 抽濾,除去濾液。在燒杯中加入Fmoc-Leu-OH 14.1 g( 40 mmol) 和DMF 100 mL,攪拌使其溶解; 加入N,N-二異丙基乙胺( DIPEA) 21 mL( 120 mmol),混合均勻后于30 ℃反應2 h。濾除液體,用DMF( 3 × 30 mL) 洗滌,加入封閉液( DCM/MeOH/DIPEA = 17 /2 /1,V /V /V) 100 mL,封閉兩次,每次10 min,依次用DMF( 5 × 20 mL) 和MeOH( 3 × 30 mL) 洗滌,每次10 min,抽濾,真空干燥過夜得Fmoc-Leu-CTCResin 28.7 g,替代度0.74 mmol·g - 1。肽鏈的延伸: 用類似的方法依次縮合Fmoc-Trp( Boc) -OH、Fmoc-Glu( OtBu) -OH、Fmoc-Val-OH、Fmoc-Arg( pbf) -OH、Fmoc-Glu( OtBu) -OH、Fmoc-Met-OH 和Fmoc-Ser ( tBu ) -OH 得肽樹脂45.8 g。全保護肽裂解: 將肽樹脂45.8 g 加入裂解液( 20%TFE /DCM) 360 mL 中,裂解2 h。抽濾,濾餅重復抽濾,合并濾液,旋蒸得3 的全保護肽31.8 g,純度94.2%; MS( ESI) m/z: 1 273.5{ [M+ H]+ } 。
3) 的全保護肽的合成
Fmoc-Asn( trt) -CTC Resin 的制備: 將2-Cl-CTC 樹脂20 g( 1.0 mmol·g - 1 ) 加入多肽合成反應柱中,加入DMF 150 mL 溶脹; 抽濾,除去濾液。在燒杯中加入Fmoc-Asn ( trt ) -OH 23.9 g ( 40mmol) 和DMF 100 mL,攪拌使其溶解; 加入DIPEA 21 mL( 120 mmol),混合均勻后加入反應柱中,于30 ℃反應2 h。濾除液體,用DMF( 3 ×30 mL) 洗滌,加入封閉液( DCM/MeOH/DIPEA =17 /2 /1,V /V /V) 100 mL,封閉兩次,每次10 min,依次用DMF( 5 × 20 mL) 和MeOH( 3 × 30 mL) 洗滌,每次10 min,抽干樹脂,真空干燥過夜得Fmoc-Asn( trt) -CTC Resin 27.2 g,替代度0.57mmol·g - 1。 肽鏈的延長: 將Fmoc-Leu-CTC Resin 26.3 g( 15 mmol) 加入反應柱中,用類似的方法依次縮合Fmoc-Leu-OH、Fmoc-His ( trt ) -OH、Fmoc-Lys( Boc) -OH 和Fmoc-Gly-OH 得肽樹脂39.8 g。全保護肽裂解: 將肽樹脂39.8 g 加入裂解液( 20%TFE /DCM) 320 mL 中,裂解2 h。抽濾,濾餅再次抽濾,合并濾液,旋蒸除溶得2 的全保護肽24.8 g,純度93.6%; MS ( ESI ) m/z: 792.3。
4)1 的全保護肽的合成
Fmoc-Leu-CTC Resin 的制備: 用類似1.2( 2)的方法制得Fmoc-Leu-CTC Resin 27.8 g,替代度0.69 mmol·g - 1。肽鏈的延長: 將Fmoc-Leu-CTC Resin 21.7 g( 15 mmol) 加入反應柱中,用類似的方法依次縮合Fmoc-Asn( trt) -OH、Fmoc-His( trt) -OH、Fmoc-Met-OH、Fmoc-Leu-OH、Fmoc-Gln ( trt ) -OH、Fmoc-Ile-OH、Fmoc-Glu ( OtBu ) -OH、Fmoc-Ser( tBu) -OH、Fmoc-Val-OH 和Fmoc-Ser ( tBu) -OH得片段肽樹脂59.3 g。
全保護肽裂解: 將肽樹脂59.3 g 加入到裂解液( 20% TFE /DCM) 480 mL 中,裂解2 h。抽濾,濾餅再次抽濾,合并濾液,旋蒸除溶得1 的全保護肽40.6 g,純度90.1%; MS( ESI) m/z: 1 494.9。
5)特立帕肽的合成
特立帕肽肽樹脂合成: 將4 的肽樹脂28.6 g( 5 mmol) 加入反應柱中,加入DMF 200 mL,溶脹30 min; 按照Fmoc 固相多肽合成原理,以HoBt /DIC 為縮合體系,20% 哌啶/DMF 溶液為脫保護試劑,DMF 為反應溶劑,2 eq.投料量,于30 ℃依次偶聯1 ~ 3 的全保護肽,偶聯3 h。茚檢若呈陽性,補加1 eq.投料至茚檢呈陰性。最后在以20% 哌啶/DMF 溶液脫除整個肽鏈氨基端的Fmoc 得特立帕肽肽樹脂56.2 g。特立帕肽粗品的制備: 將特立帕肽肽樹脂56.2 g( 5 mmol) 加入裂解液( TFA/EDT /TIS /間甲酚= 92.5 /2.5 /2.5 /2.5,V /V /V /V( 450 mL) 中,裂解2.5 h。抽濾,濾餅用TFA( 2 × 100 mL) 洗滌,合并濾液和洗液( 670 mL),加入冰異丙醚4L,沉降,離心,棄上清液,用異丙醚( 3 × 300 mL)洗滌,真空干燥過夜得特立帕肽粗品29.6 g。特立帕肽純品制備: 將特立帕肽粗品29.6 g( 5 mmol) 溶解于純水( 2.5 L) 中,于40 ℃攪拌至HPLC 檢測雙峰消失,再經制備型P-HPLC 純化,收集、合并純度大于99% 的樣品,用醋酸銨脫鹽后,濃縮、凍干得純品特立帕肽6.8 g。
[1] CN201510295556.2 一種合成特立帕肽的方法
[2] 特立帕肽治療骨質疏松癥的應用進展
[3] 片段法合成抗骨質疏松多肽藥物特立帕肽